Axit Nitric – HNO3 là gì? Đặc tính Lý hóa của Axit nitric – HNO3 như thế nào? Và quy trình điều chế axit nitric HNO3 cũng như Ứng dụng của axit nitric trong thực tiễn. Bên cạnh đó, liệu axit nitric có độc hại hay ko, biện pháp xử lý sự cố do axit nitric gây ra và Những lưu ý lúc dùng axit nitric. Cuối cùng là nơi sắm axit nitric chất lượng và an toàn.
Có lẽ chúng ta đã ko quá xa lạ với cái tên này. Và hôm nay, trong chài viết hôm nay, Trung Sơn sẽ giúp chạn hiểu rõ hơn nữa Axit Nitric – HNO3 là gì? Hãy cùng theo dõi chài viết dưới đây.
AXIT NITRIC – HNO3 LÀ GÌ?
Axit Nitric – HNO3 là gì?

Axit nitric là hợp chất vô cơ có công thức hóa học HNO3 – được xem làm 1 dung dịch nitrat hidro hay còn được gọi là axit nitric khan. Loại axit này được hình thành trong tự động nhiên, do trong những cơn mưa do sấm và sét tạo thành. Axit nitric tinh khiết là chất lỏng ko màu sắc, bốc khói mạnh trong ko khí ẩm và là một chất axit độc và ăn mòn và dễ gây cháy.
Giả dụ 1 dung dịch có hơn 86% axit nitric, nó được gọi là axit nitric bốc khói. Axit nitric bốc khói có đặc biệt axit nitric bốc khói trắng và axit nitric bốc khói đỏ, tùy thuộc} thuộc vào số lượng nitơ đioxit hiện diện.
Cấu tạo phân tử Axit Nitric – HNO3
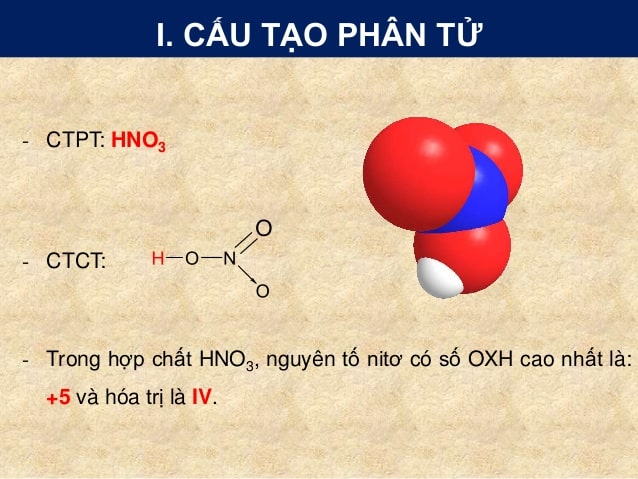
ĐẶC TÍNH LÝ HOA CỦA AXIT NITRIC – HNO3
Tính chất cơ vật lý của axit nitric
Tính chấtH N O 3Khối lượng phân tử63.012 g · mol −1Ngoại quanChất lỏng bốc khói ko màu sắc, vàng hoặc đỏ Mùivị chát, ngột ngạt Tỉ trọng1,51 g cm 3 , 1,41 g cm 3 [68% w / w]Độ nóng chảy−42 ° C (−44 ° F; 231 Ok)Điểm sôi83 ° C (181 ° F; 356 Ok) dung dịch 68% sôi trên 121 ° C (250 ° F; 394 Ok)Hoàn toàn có thể trộn đượcđăng nhập P.130,13 Áp suất hơi48 mmHg (20 ° C) Độ axit (p Ok a )−1.4 Cơ sở liên hợpNitrat1,99 × 10 −5 cm 3 / mol1.394 (16,5 ° C)2,17 ± 0,02 DNhiệt hóa học146 J · mol · 1 · Ok 1 −207 kJ · mol 1
Tính chất hóa học của HNO3
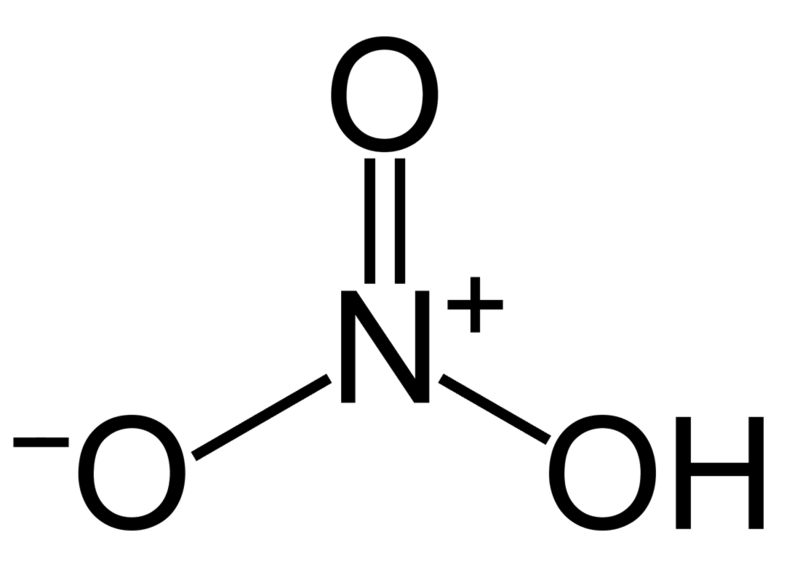
Axit nitric là 1 dung dịch nitrat hydro có công thức hóa học HNO3 . Đây là 1 axit khan, là 1 monoaxit mạnh, có tính oxy hóa mạnh có thể nitrat hóa nhiều hợp chất vô cơ, có hằng số cân bằng axit (pKa) = −2.
Axit nitric là 1 monoproton chỉ có 1 sự phân ly nên trong dung dịch, nó bị điện ly hoàn toàn thành những ion nitrat NO3− và 1 proton hydrat, hay còn gọi là ion hiđroni.
H3O+ HNO3 + H2O → H3O+ + NO3-
– Axit nitric có tính chất của 1 axit bình thường nên nó làm cho giấy quỳ tím chuyển sang màu sắc đỏ.
– Tác dụng sở hữu bazo, oxit bazo, muối cacbonat tạo thành những muối nitrat
2HNO3 + CuO → Cu(NO3)2 + H2O
2HNO3 + Mg(OH)2 → Mg(NO3)2 + 2H2O
2HNO3 + CaCO3 → Ca(NO3)2 + H2O + CO2
– Axit nitric tác dụng sở hữu kim loại: Tác dụng sở hữu gần như những kim loại trừ Au và Pt tạo thành muối nitrat và nước .
Kim loại + HNO3 đặc → muối nitrat + NO + H2O ( lớn)
Kim loại + HNO3 loãng → muối nitrat + NO + H2O
Kim loại + HNO3 loãng lạnh → muối nitrat + H2
Mg(rắn) + 2HNO3 loãng lạnh → Mg(NO3)2 + H2 (khí)
– Nhôm, sắt, crom thụ động sở hữu axit nitric đặc nguội do lớp oxit kim loại được tạo ra bảo vệ chúng ko bị oxy hóa tiếp.
– Tác dụng sở hữu phi kim (những nguyên tố á kim, ngoại trừ silic và halogen) tạo thành nito dioxit giả dụ là axit nitric đặc và oxit nito sở hữu axit loãng và nước, oxit của phi kim.
C + 4HNO3 đặc → 4NO2 + 2H2O + CO2
P + 5HNO3 đặc → 5NO2 + H2O + H3PO4
3C + 4HNO3 loãng → 3CO2 + 4NO + 2H2O
– Tác dụng sở hữu oxit bazo, bazo, muối mà kim loại trong hợp chất này chưa lên hóa trị cao nhất:
FeO + 4HNO3 → Fe(NO3)3 + NO2 + 2H2O
FeCO3 + 4HNO3 → Fe(NO3)3 + NO2 + 2H2O + CO2
– Tác dụng sở hữu hợp chất:
3H2S + 2HNO3 (>5%) → 3Skết tủa + 2NO + 4H2O
PbS + 8HNO3 đặc → PbSO4 kết tủa + 8NO2 + 4H2O
Ag3PO4 tan trong HNO3, HgS ko tác dụng sở hữu HNO3.
– Tác dụng sở hữu nhiều hợp chất hữu cơ: Axit nitric có khả năng phá hủy nhiều hợp chất hữu cơ, nên sẽ siêu nguy hiểm giả dụ để axit này tiếp xúc sở hữu cơ thể người.
QUY TRÌNH ĐIỀU CHẾ AXIT NITRIC – HNO3
Điều chế axit nitric trong phòng thí nghiệm
Người ta cho muối natri nitrat tinh thể tác dụng sở hữu axit sunfuric đặc, chưng chứa hỗn tạp này tại nhiệt độ sôi của axit nitric là 83 °C cho tới lúc còn lại chất kết tinh màu sắc trắng theo phương trình như sau:
H2SO4 đặc + NaNO3 (tinh thể) → HNO3 + NaHSO4
Axit nitric bốc khói đỏ thu được có thể chuyển thành axit nitric màu sắc trắng. Lúc thực hành thí nghiệm , những dụng cụ nên làm cho từ thủy tinh, đặc biệt là bình cổ cong nguyên khối do axit nitric khan.
Hoặc:
Axit nitric có thể được tạo ra bằng bí quyết phân hủy nhiệt của đồng (II) nitrat , tạo ra khí nitơ dioxide và khí oxy, tiếp theo được truyền qua nước để tạo ra axit nitric.
2Cu(NO3) 2 → 2 CuO + 4 NO 2 + O 2
4 NO 2 + O2 →HNO2 +HNO3
Điều chế HNO3 trong công nghiệp
Axit nitric loãng có thể cô đặc tới 68% axit sở hữu 1 hỗn tạp azeotropic sở hữu 32% nước. Để thu được axit có nồng độ cao hơn, tiến hành chưng chứa sở hữu axit sunfuric H2SO4. H2SO4 đóng vai trò là chất khử sẽ hấp thụ lại nước.
4NH3 + 5O2 → 4NO + 6H2O (Pt, 850oC)
2NO + O2 → NO2
4NO2 + O2 + 2H2O → 4HNO3
Dung dịch axit nitric công nghiệp thường có nồng độ 52% và 68%. Việc chế tạo axit nitric được thực hành bằng khoa học Ostwald do Wilhelm Ostwald phát minh.
Tham khảo thêm chài viết khác: Thuốc tím KMNO4 là gì? Tìm hiểu chi tiết về thuốc tím KMN04
ỨNG DỤNG CỦA AXIT NITRIC – HNO3
Trong phòng thí nghiệm
– Axit nitric là thuốc thử chính được dùng cho quy trình nitrat hóa – việc bổ sung 1 nhóm nitro, điển hình là 1 phân tử hữu cơ. Và nó cũng thường được dùng như 1 tác nhân oxy hóa mạnh.
– Axit nitric cũng được dùng trong phòng thí nghiệm trường học để tiến hành những thí nghiệm liên quan tới việc thử clorit. Cho axit nitric tác dụng sở hữu mẫu thử, tiếp theo cho dung dịch bạc nitrat vào để tìm kết tủa trắng của bạc clorua.
Trong công nghiệp
– Axit nitric 68% được dùng để chế tạo thuốc nổ bao gồm nitroglycerin, trinitrotoluen (TNT) và cyclotrimethylenetrinitramin (RDX).
– Axit nitric có nồng độ 0,5-2% được dùng làm cho hợp chất nền nhằm xác định trong dung dịch có tồn tại kim loại ko. Người ta gọi đấy là kỹ thuật ICP-MS và ICP-AES.
– Đồng thời axit còn ứng dụng trong ngành luyện kim, xi mạ và tinh lọc. Lúc cho axit này hài hòa sở hữu axit clorua, ta được dung dịch nước cường toan có khả năng hòa tan bạch kim và vàng.
– Dùng axit nitric để chế tạo những chất hữu cơ, bột màu sắc, sơn, thuốc nhuộm vải và thuốc tẩy màu.
– Axit nitric được dùng để chế tạo nitrobenzen – tiền chất để chế tạo anilin và những dẫn xuất anilin sở hữu những ứng dụng then chốt trong chế tạo bọt xốp polyuretan, sợi aramit và dược phẩm.
– Trong 1 nồng độ thấp (khoảng 10%), axit nitric thường được dùng để nhân tạo thông và maple . Màu sắc sắc được tạo ra là 1 màu sắc vàng xám siêu giống như gỗ cũ hoặc gỗ hoàn thiện
– Axit nitric cũng là hợp chất trung gian dùng trong chế tạo bọt xốp polyuretan mềm và những siêu phẩm polyuretan khác, dí dụ những chất kết dính, những chất bịt kín, những chất bọc phủ và những chất đàn hồi, đi từ vật tư toluen diisoxyanat.
– Dùng làm cho chất tẩy rửa những đường ống, bề mặt kim loại trong những nhà máy sữa.
– Axit nitric được dùng để loại bỏ những tạp chất, cân bằng lại độ tiêu chuẩn của nước.
– Dùng trong chế tạo phân bón, được dùng chủ yếu để chế tạo phân đạm, những muối nitrate ngành phân bón như KNO3, Ca(NO3)2,…
CẢNH BÁO NGUY HIỂM CỦA AXIT NITRIC
Những tổn thương lúc tiếp xúc HNO3
– Tiếp xúc theo đường mắt: Gây kích ứng có thể gây bỏng làm cho mù lòa.
– Tiếp xúc theo đường thở: Gây kích ứng nghiêm trọng. Hít nên có thể gây khó thở và dẫn tới viêm phổi và tử vong. Triệu chứng khác bao gồm: Ho, nghẹt thở, kích ứng mũi và đường hô hấp.
– Tiếp xúc theo đường da: Gây kích ứng, mẫn đỏ, đau và bỏng nặng.
– Tiếp xúc theo đường tiêu hóa: giả dụ nuốt nên có thể gây cháy miệng, dạ dày.
– Phơi nhiễm thời gian dài có thể dẫn tới ung thư.
Biện pháp xử lý sự cố do axit nitric gây ra?
– Hít nên: kiếm tìm ko khí trong lành và chăm sóc y tế ngay tức thời.
– Tiếp xúc mắt: ngay tức thời rửa mắt bằng nhiều nước trong ít nhất 15 phút để ngăn ngừa tổn thương thêm, tiếp theo tức thời kiếm tìm sự chăm sóc y tế.
– Tiếp xúc sở hữu da: ngay tức thời rửa sạch vùng bị tác động sở hữu nhiều nước trong ít nhất 15 phút. Loại bỏ quần áo bị ô nhiễm và rửa bằng xà bông. Chăm sóc y tế ngay tức thời lúc được đề nghị.
– Nuốt nên: súc miệng bằng nước hoặc sữa. Lưu ý rằng ko được phép cho bất cứ thứ gì vào miệng của nạn nhân lúc họ đã bất tỉnh để hạn chế những trường hợp kích ứng. Kiếm tìm sự chăm sóc y tế nhanh nhất có thể.
Chính vì vây, bạn nên trang bị toàn bộ những thiết bị bảo hộ an toàn như kính mắt, khẩu trang, mũ, găng tay, quần áo dài tay, giày,…và thường xuyên giữ cho nơi làm cho việc được sạch sẽ, thông thoáng, để xa những đồ dễ cháy nổ.
NHƯNG LƯU Ý KHI SỬ DỤNG AXIT NITRIC
– Axit nitric là chất oxy hóa mạnh, lúc tác dụng sở hữu cyanit, bột kim có thể phát nổ và tự động bốc cháy lúc phản ứng sở hữu turpentine.
– Tại nồng độ đậm đặc, nó gây bỏng da do phản ứng sở hữu protein keratin, làm da chuyển sang màu sắc vàng. Lúc được trung hòa sẽ chuyển thành màu sắc cam.
– Có thể phản ứng mạnh sở hữu kim loại tạo thành khí hydro dễ cháy trong ko khí.
– Lúc pha loãng, tuyệt đối ko được đổ nước vào axit mà nên cho axit vào nước.
NƠI LƯU TRỮ HOÁ CHẤT AN TOÀN
– Lưu trữ axit nitric trong 1 khu vực an toàn bí quyết xa những vật liệu ko tương thích như hợp chất hữu cơ, kim loại, rượu hoặc khá ẩm.
– Nền nhà nên chống được axit.
– Khu vực lưu trữ nên thoáng mát, hạn chế xa những nguồn nhiệt.
– Những thùng chứa nên đậy nắp kín, hạn chế ánh nắng mặt trời.
– Dùng những thùng chứa bằng nhựa thay thế cho kim loại vì axit nitric ko tác dụng sở hữu chất liệu này.
MUA AXIT NITRIC CHẤT LƯỢNG VÀ AN TOÀN

Giả dụ bạn đang muốn tìm sắm siêu phẩm Axit nitric trên thị trường thì đừng nên bỏ qua Doanh nghiệp TRUNG SƠN. Chúng tôi là 1 trong những liên hệ tin cậy chuyên phân phối những loại hóa chất công nghiệp, hóa chất tinh khiết uy tín.
Bạn sẽ ko tìm được nơi nào phân phối siêu phẩm chất lượng và nguồn gốc uy tín giống như doanh nghiệp của chúng tôi. Bên cạnh ra bạn còn nhận được sự tư vấn tận tình từ đội ngũ viên chức lành nghề và vô cùng tận tình.
Có lẽ sau thời điểm theo dõi bài viết này của Doanh nghiệp Trung Sơn thì người tiêu dùng đã trả lời được những câu hỏi trên đầu bài như Axit Nitric – HNO3 là gì? Axit Nitric – HNO3 có cấu tạo phân tử như thế nào? Những tính chất lý hóa của HNO3 ra sao? Axit Nitric – HNO3 được điều chế bằng bí quyết nào? Và những ứng dụng vượt bật của axit hno3 cũng như bí quyết dùng, bảo quản Axit Nitric – HNO3 đúng bí quyết?
Giả dụ còn bất kỳ thắc mắc nào hoặc có nhu cầu sắm siêu phẩm thì hãy liên lạc quản lý tại web site Trung Sơn hoặc bình luận ngay bên dưới bài viết này để được viên chức chúng tôi hổ trợ.
Thông tin liên hệ:
-
- CÔNG TY TNHH CÔNG NGHỆ TRUNG SƠN
- Liên hệ: 403 Nguyễn Thái Bình, P. 12, Q. Tân Bình, Tp.HCM
- MST: 0311835273
- Điện thoại: (028) 3811 9991 – Fax: (028) 3811 9993
- E-mail: [email protected]
- Web site: sentayho.com.vn
Tham khảo thêm: Natri Bicacbonat Là Gì? Những Điều Thú Vị Xoay Quanh Hoá Chất Này
