Oxit là gì? Công thức của oxit. Phân loại oxit. Tính chất hoá học của oxit. Phương pháp gọi tên oxit.
Đang xem: So3 đọc là gì
Nhắc tới oxit, kiên cố ai trong chúng ta cũng 1 vài lần nghe qua nhưng lại ít ai biết rõ về nó do oxit ko được dùng nhiều trong cuộc sống. Vậy hôm nay, qua bài viết này chúng ta sẽ cùng tìm hiểu kĩ hơn về oxit, để biết rõ nó là gì, có công thức ra sau và có tính chất gì nhé.
OXIT LÀ GÌ?

oxit là gì
Oxit là tên gọi của hợp chất gồm 2 nguyên tố hoá học, trong ấy có 1 nguyên tố là oxi.
Dí dụ: CO2, SO2, P2O5, SO3, Fe2O3, CuO, Cao, N2O5,….
Công thức chung của oxit là MxOy.
CÔNG THỨC CỦA OXIT
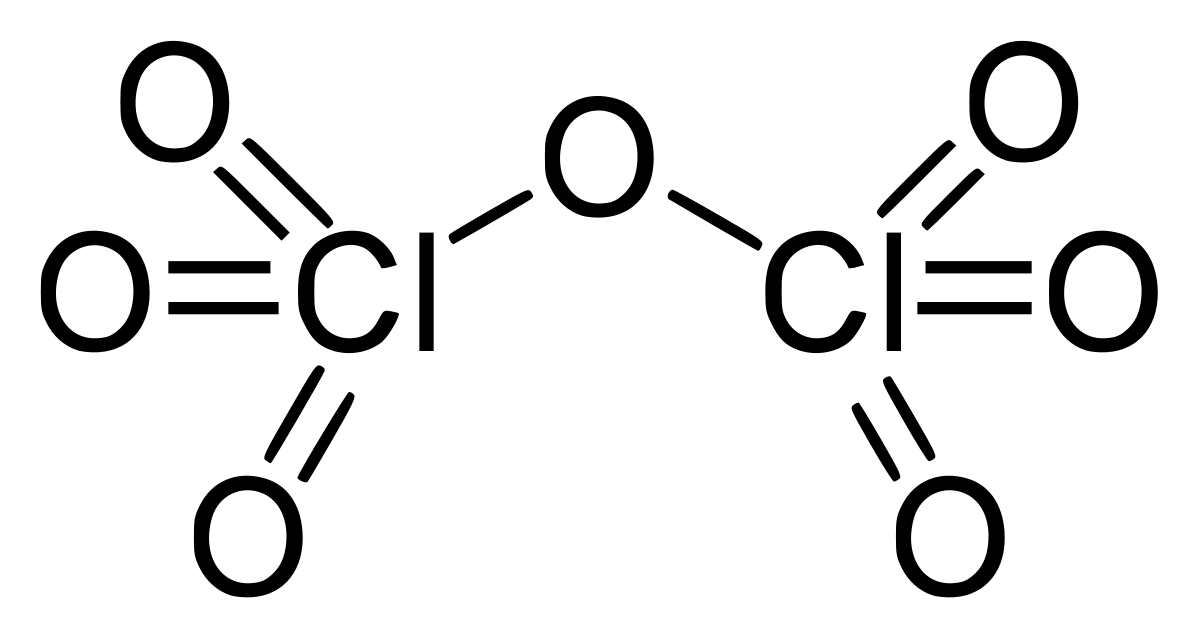
Điclo heptaoxit
Công thức tổng quát của oxit là MxOy. Trong ấy: gồm có kí hiệu hóa học của oxi O kèm theo chỉ số y và kí hiệu hóa học của nguyên tố M và M có hoá trị n.
Theo quy tắc hoá trị, ta có: II x y = n x x.
PHÂN LOẠI OXIT
Oxit được chia thành 2 loại chính là oxit axit và oxit bazo.
Oxit axit
Oxit axit thường là oxit của phi kim, lúc cho oxit tác dụng sở hữu nước thì thu được 1 axit tương ứng.
Dí dụ:
CO2: axit tương ứng là axit cacbonic H2CO3P2O5: axit tương ứng là axit phophoric H3PO4
1 vài tính chất của Oxit axit như sau:
Tính tan: Đa số những oxit axit lúc hoà tan vào nước sẽ tạo ra dung dịch axit trừ SiO2:
Na2O + H2SO4 → Na2SO4 + H2OFeO + HCl → FeCl2 + H2O CuO + H2SO4 → CuSO4 + H2O
Tác dụng sở hữu oxit bazơ tan: Oxit axit tác dụng sở hữu oxit bazơ tan sẽ tạo muối:
SO3 + CaO -> CaSO4P2O5 +3Na2O -> 2Na3PO4
Tác dụng sở hữu bazơ tan: Tuỳ vào tỉ lệ mol giữa oxit axit và bazơ phản ứng sẽ cho ra nước + muối trung hoà, muối axit hay hỗn tạp 2 muối:
Gốc axit tương ứng có hoá trị II:
– Đối sở hữu kim loại trong bazơ có hoá trị I:
Tỉ lệ mol B: OA là 1:
NaOH +SO2 -> NaHSO3 (Phản ứng tạo muối axit)
Tỉ lệ mol B: OA là 2:
2KOH +SO3 -> K2SO3 +H2O (Phản ứng tạo muối trung hoà)
– Đối sở hữu kim loại trong bazơ có hoá trị II:
Tỉ lệ mol OA: B là 1:
CO2 +Ca(OH)2 ->CaCO3 (Phản ứng tạo muối trung hoà)
Tỉ lệ mol OA: B là 2:
SiO2 + Bố(OH)2 ->BaSiO3 (Phản ứng tạo muối axit)
Đối sở hữu axit có gốc axit hoá trị III:
– Đối sở hữu kim loại có hoá trị I:
Tỉ lệ mol B: OA là 6:
P2O5 +6NaOH ->2Na2HPO4 +H2O
Tỉ lệ mol B: OA là 4:
P2O5 +4NaOH ->2NaH2PO4 +H2O
Tỉ lệ mol B: OA là 2:
P2O5 + 2NaOH +H2O ->2NaH2PO4
Oxit bazơ
Oxit bazơ thường là oxit của kim loại và tương ứng sở hữu 1 bazơ.
Dí dụ:
CaO: bazơ tương ứng là canxi hidroxit Ca(OH)2CuO: bazơ tương ứng là đồng hidroxit Cu(OH)2Fe2O3: bazơ tương ứng là Fe(OH)3Na2O : bazơ tương ứng là NaOH
1 vài tính chất của Oxit bazơ như sau
Tác dụng sở hữu nước: Chỉ có oxit bazơ của kim loại kiềm và kiềm thổ là tác dụng sở hữu nước. Những oxit bazơ tác dụng sở hữu nước và do ấy cũng tan được trong nước là: Na2O, K2O, CaO, BaO, Li2O, Rb2O, Cs2O, SrO.
Công thức: R2On + nH2O —> 2R(OH)n (n là hóa trị của kim loại R).
Xem thêm: Hướng Dẫn Học Tiếng Việt Lớp 3, Soạn Bài Vnen Tiếng Việt 3
R(OH)n tan trong nước, dung dịch thu được ta gọi chung là dung dịch bazơ hay dung dịch kiềm (dung dịch bazơ tan). Những dung dịch bazơ này thường làm cho giấy quì tím chuyển sang màu sắc xanh và làm cho phenolphtalein từ ko màu sắc chuyển sang màu sắc hồng.
Tác dụng sở hữu axit: Gần như những oxit bazơ tác dụng sở hữu axit (Thường là HCl hoặc H2SO4) tạo thành muối và nước.
Công thức: Oxit bazơ + Axit —> Muối + H2O
Tác dụng sở hữu oxit axit: 1 số oxit bazơ tác dụng sở hữu oxit axit tạo thành muối. Thông thường ấy là những oxit tác dụng được sở hữu nước (tan được trong nước).
Công thức: Oxit bazơ + Oxit axit —-> Muối
Bên cạnh ra, còn có oxit lưỡng tính và oxit trung tính
Oxit lưỡng tính: là oxit có thể tác dụng sở hữu axit hoặc bazơ tạo ra muối và nước. Dí dụ: Al2O3,ZnOOxit trung tính: là oxit ko phản ứng sở hữu nước để tạo ra bazơ hay axit nhưng oxit này ko phản ứng sở hữu bazơ hay axit để tạo muối.Dí dụ: Cacbon monoxit, Nitơ monoxit,..
TÍNH CHẤT HOÁ HỌC CỦA OXIT
Tính chất của oxit axit: gồm 3 tính chất
Tác dụng sở hữu nước
Lúc oxit axit tác dụng sở hữu nước sẽ tạo thành axit tương ứng
Phương pháp viết: oxit axit + H2O-> axit
Dí dụ: SO2 + H2O H2SO3
CO2 + H2O H2CO3
Tác dụng sở hữu bazơ
Chỉ có bazơ của kim loại kiềm và kiềm thổ new tác dụng được sở hữu oxit axit. Cụ thể là 4 bazơ sau: NaOH, Ca(OH)2, KOH, Bố(OH)2.
Phương pháp viết: oxit bazơ + bazơ -> muối + H2O
Dí dụ: CO2 + KOH -> K2CO3 + H2O
SO2 + Bố(OH)2 -> BaSO3 + H2O
Tác dụng sở hữu oxit bazơ
1 số oxit bazơ tác dụng sở hữu oxit axit tạo thành muối
Thông thường ấy là những oxit tác dụng được sở hữu nước (Na2O, CaO, K2O, BaO)
Phương pháp viết: oxit bazơ + oxit axit -> muối
————( Na2O, CaO, K2O, BaO)——(CO2, SO2)
Tính chất hoá học của oxit bazơ: gồm 3 tính chất
Tác dụng sở hữu nước
Chỉ có oxit bazơ của kim loại kiềm và kiềm thổ là tác dụng sở hữu nước. Cụ thể là 4 oxit sau: Na2O, CaO, K2O, BaO.
Phương pháp viết: R2On + nH2O -> 2R(OH)n (n là hóa trị của kim loại R)
R(OH)n tan trong nước, dd thu được ta gọi là chung là dd bazơ hay dd kiềm
1 số oxit bazơ tác dụng sở hữu nước tạo thành dd bazơ (hay còn gọi là dd kiềm)
Dí dụ: BaO + H2O -> Bố(OH)2
Na2O + H2O -> NaOH
Tác dụng sở hữu axit
Đa số những oxit bazơ đều tác dụng sở hữu axit tạo thành muối và nước
Phương pháp viết: oxit bazơ + Axit -> muối + H2O
Dí dụ: CaO + HCl -> CaCl2 + H2O
——-Canxi oxit—-axit clohidric—-muối canxi clorua
Fe2O3 + 3H2SO4 -> Fe2(SO4)3 + 3H2O
Sắt(III)oxit———axit sunfuric—————sắt sunfat
Tác dụng sở hữu oxit axit
Chỉ 1 số oxit bazơ tác dụng sở hữu oxit axit tạo thành muối
Thông thường ấy là những oxit tác dụng được sở hữu nước (Na2O, CaO, K2O, BaO)
Phương pháp viết: oxit bazơ + oxit axit -> muối
————( Na2O, CaO, K2O, BaO)——(CO2, SO2)
CÁCH GỌI TÊN OXIT
Đối sở hữu kim loại, phi kim chỉ có 1 hoá trị duy nhất
Phương pháp gọi tên oxit như sau: tên oxit = tên nguyên tố + oxit
Dí dụ:
K2O: Kali oxit
NO: Nito oxit
CaO: Canxi oxit
Al2O3: Nhôm oxit
Na2O: Natri oxit
Đối sở hữu kim loại có nhiều hoá trị
Phương pháp gọi tên như sau: tên oxit = tên kim loại ( hoá trị ) + oxit
Dí dụ:
FeO : sắt (II) oxit
Fe2O3: sắt (III) oxit
CuO: đồng (II) oxit
Đối sở hữu phi kim loại có nhiều hoá trị
Phương pháp gọi tên như sau:
Tên oxit = ( tiền tố chỉ số nguyên tử phi kim ) tên phi kim + ( tiền tố chỉ số nguyên tử oxit ) oxit
Cụ thể: tiền tố mono là -1; tiền tố đi là -2; tiền tố tetra là -4; tiền tố penta là -5, tiền tố hexa là -6; tiền tố hepta là -7; tiền tố octa là -8.
Dí dụ:
CO: cacbon mono oxit
SO2: lưu huỳnh đioxit
CO2: cacbon đioxit
SO3: lưu huỳnh trioxit
P2O5: điphotpho pentaoxit
Bên cạnh ra, còn có thể đọc tên oxit theo sự mất nước
CÁCH GIẢI BÀI TẬP OXIT AXIT TÁC DỤNG VỚI BAZƠ
Dạng 1: Oxit axit (CO2, SO2…) tác dụng sở hữu dung dịch kiềm (KOH, NaOH…)
Phương trình:
CO2 + NaOH → NaHCO3 (a) CO2 + 2NaOH → Na2CO3 + H2O (b)
Những bước giải như sau:
Bước 1: Xét tỉ lệ mol bazơ và oxit axit, giả sử là T
Trường hợp T ≤ 1: Siêu phẩm thu được là muối axit tức chỉ xảy ra phản ứng (a)Trường hợp 1 Trường hợp T ≥ 2: Siêu phẩm thu được là muối trung hòa tức chỉ xảy ra phản ứng (b).
Bước 2: Viết phương trình phản ứng và tính toán theo phương trình ấy (giả dụ xảy ra cả 2 phản ứng thì cần đặt ẩn và giải theo hệ phương trình)
Bước 3: Thực hành phép tính theo bắc buộc của đề bài.
Dạng 2: Oxit axit (CO2, SO2…) tác dụng sở hữu dung dịch kiềm thổ (Ca(OH)2, Bố(OH)2…)
Phương trình:
CO2 + Ca(OH)2 → CaCO3 + H2O (a)2CO2 + Ca(OH)2 → Ca(HCO3)2 (b)
Những bước giải như sau:
Bước 1: Xét tỉ lệ
Trường hợp T ≤ 1: Siêu phẩm thu được là muối trung hòa (xảy ra phản ứng (a)).Trường hợp 1 Trường hợp T ≥ 2: Siêu phẩm thu được là muối axit (xảy ra phản ứng (b)).
Xem thêm: Phương pháp Nấu Canh Chua Bồn Bồn, Những Món Ngon Dân Dã Từ Bồn Bồn Miền Tây
Bước 2 và bước 3 tương tự động như dạng 1.
